-
探讨心室纤颤的不同病因机制(针对基础医学专业的拓展模块)
-
心室纤颤病人的复苏后处理(针对临床医学专业的拓展模块)
-
转录组学技术寻找心源性猝死的病理学标志物针对法医专业的拓展模块)
-
乌头碱诱发快速室性心律失常模型
-
实验内容
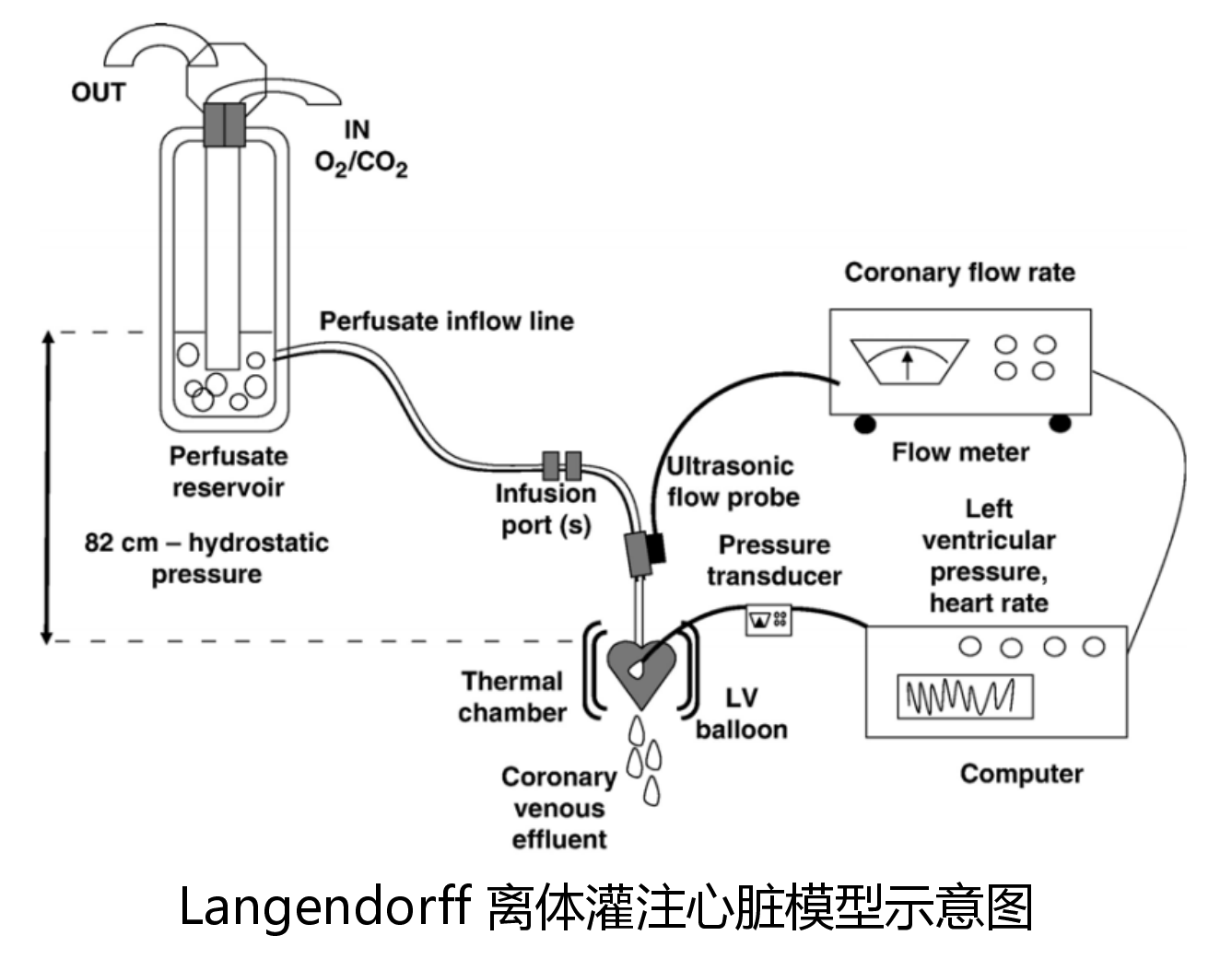
心室纤颤的发生往往与基础性疾病相关,冠心病是最常见的基础性疾病。心室纤颤患者成功复苏后,都需要针对基础疾病进行针对性治疗。本实验利用虚拟数字人,模拟冠心病患者心室纤颤复苏后的介入或手术治疗。
-
实验背景
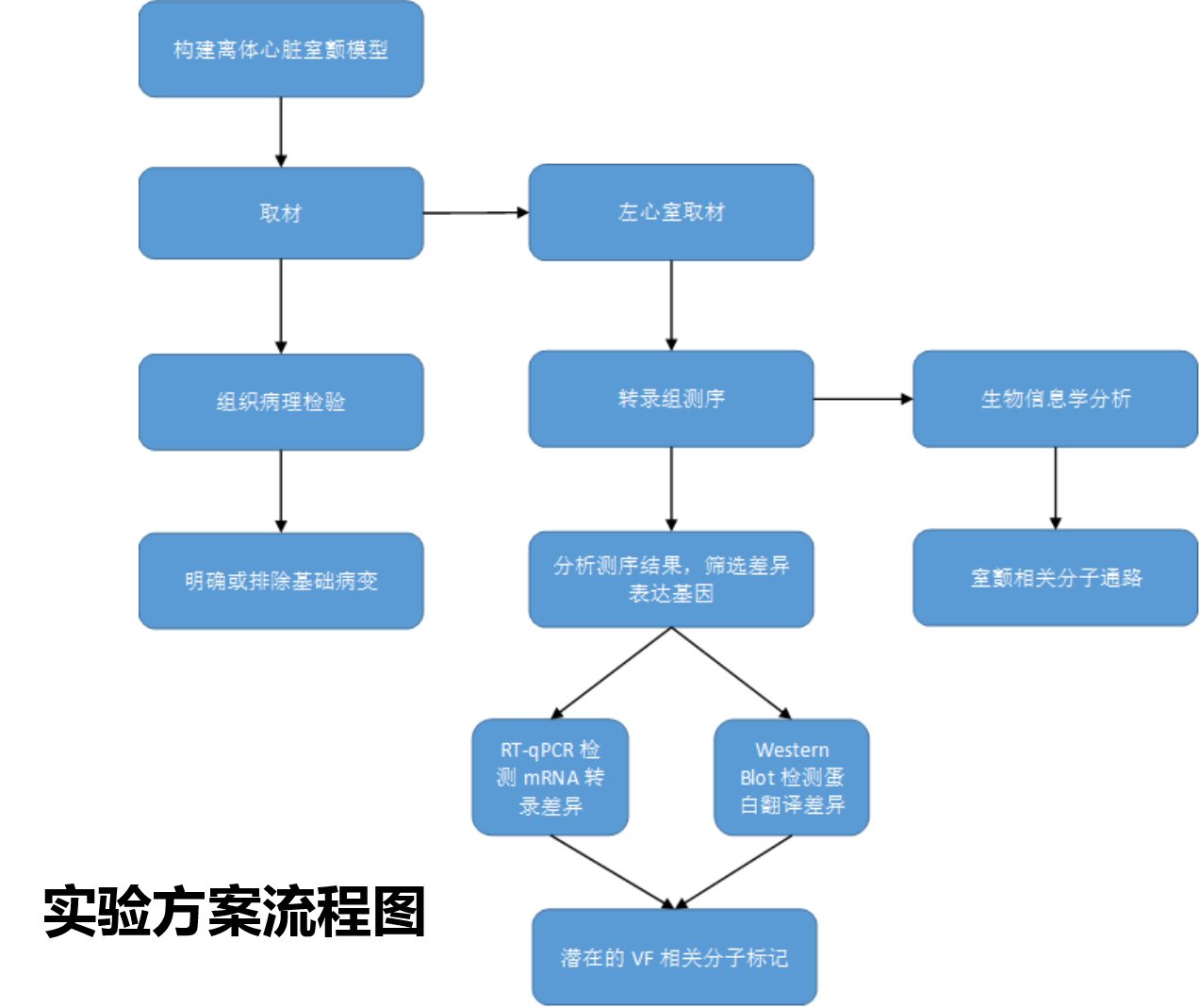
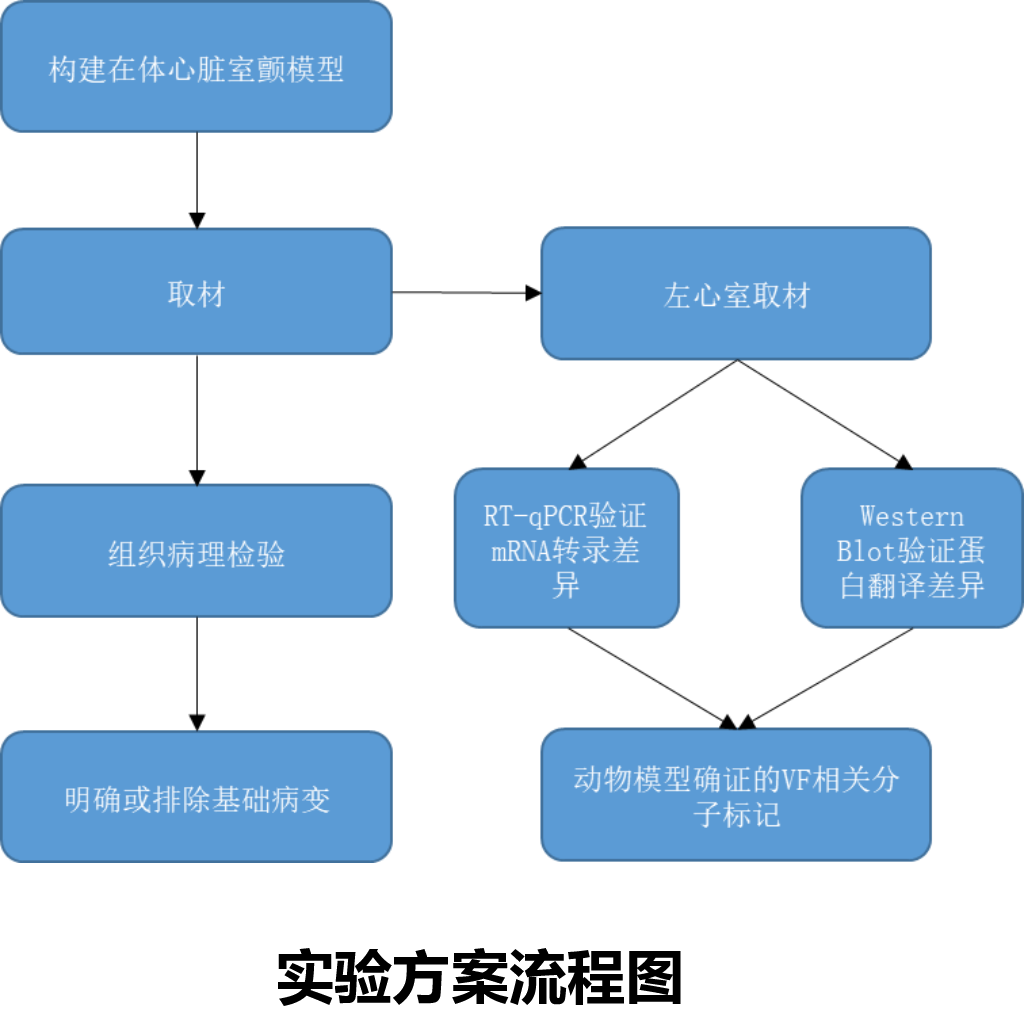
实验方案
心源性猝死(SCD)是指在没有明显的非心脏性原因的情况下,在症状出现后1h内(witnessed)或生前最后一次被观察到处于健康状态后24小时内(unwitnessed)发生的猝死
流行病学数据:
美国:180,000-450,000人/年
中国:约600,000人/年
病因:
1.结构性心脏病:冠心病、扩张性心肌病、肥厚型心肌病、致心率失常型右室心肌病、瓣膜疾病、炎性疾病、浸润疾病等
2.非结构性心脏病:LQTS、 SQTS、BrS、CPVT、IVT等
危险因素:年龄、种族、性别、环境、情绪应激、生活习惯
心源性猝死(SCD)是指在没有明显的非心脏性原因的情况下,在症状出现后1h内(witnessed)或生前最后一次被观察到处于健康状态后24小时内(unwitnessed)发生的猝死
流行病学数据:
美国:180,000-450,000人/年
中国:约600,000人/年
病因:
1.结构性心脏病:冠心病、扩张性心肌病、肥厚型心肌病、致心率失常型右室心肌病、瓣膜疾病、炎性疾病、浸润疾病等
2.非结构性心脏病:LQTS、 SQTS、BrS、CPVT、IVT等
危险因素:年龄、种族、性别、环境、情绪应激、生活习惯
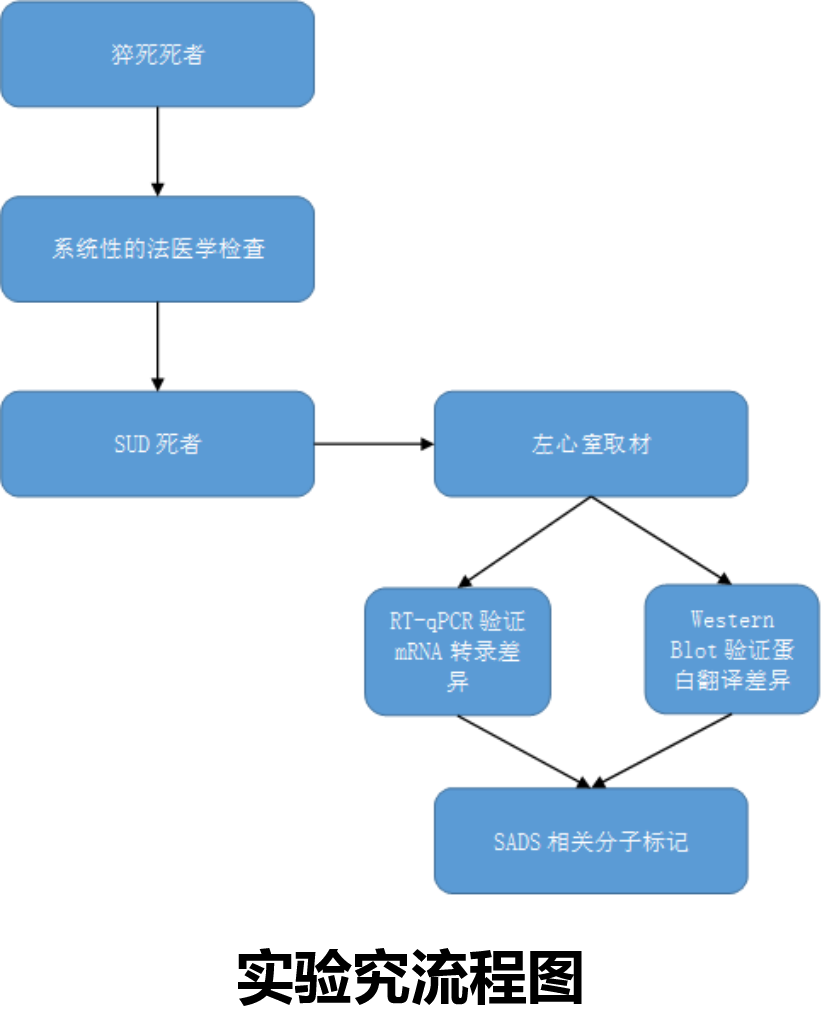
心源性猝死的法医学检验:
全面的尸体解剖、情况调查、病史回顾。尸体解剖和组织学检验发现心脏疾病的证据,排除非心脏性死因。
不明原因猝死(SUD):排除非心脏性死因,解剖检验无心脏病理性改变或病变轻微、毒物检验阴性的心源性猝死。即心率失常猝死综合征(SADS)。
发生率:
一般人群:全部SCD的5%-10%
年轻人群:全部SCD的3%-30%
中国人群:6.1%-15.1%
病因:未知
可能与离子通道病、心肌病、心肌炎、遗传性结缔组织病、传导疾病、营养状况、代谢障碍和药物
问题和挑战:
SUD死者的死亡是否为心脏原因导致?
如何为这类死亡的法医学诊断提供客观的依据?
SUD与分子解剖
离子通道病:基因缺陷引起心肌细胞离子通道结构和功能的异常,导致心率失常和猝死
特点:遗传模式复杂、发病隐匿、后果严重
分子解剖:利用分子生物学技术对SUD死者进行致病基因检测以明确其死因
局限:
1.低阳性率,约70%的SUD不能通过分子解剖得到解释
2.受限于检测成本、伦理、法律等因素,难以普及
SCD的分子标记
1.大鼠急性心肌缺血早期左心室CTSL mRNA升高
2.Hba1/2、Hbb在SCD死者左心室中表达水平升高,Pdk4表达水平下降
展示了SCD分子层面的变化,但不能真正解决SUD的法医学鉴定问题
提示:生物分子的变化可能为SUD的死因鉴定提供证据
困难:复杂的病因基础和危险因素为分子标记的筛选带来困难
文献检索发现:
1.室颤(Ventricular Fibrillation, VF)是SCD发生的重要机制(80%左右,近年有所下降)
2.VF是多数离子通道病引起死亡的共同机制
3.VF可以引起某些基因表达的下调
假设:
VF代表了多数SCD终末期的心脏节律状态,VF反应性的分子标记能够提示死者生前的心脏活动情况,从而为SUD的法医学诊断提供客观依据